728x90
반응형
- 실험 방법
➀ 다음 표와 같은 용액을 조재한다.
반응 |
100mL 삼각 플라스크 |
50mL 비커 |
|||
0.2M KI |
0.05M |
녹말용액 |
0.2M KCl |
0.2M |
|
1 |
10.0mL |
5.0mL |
1.0mL |
24.0mL |
10.0mL |
2 |
10.0mL |
5.0mL |
1.0mL |
14.0mL |
20.0mL |
3 |
10.0mL |
5.0mL |
1.0mL |
4.0mL |
30.0mL |
4 |
20.0mL |
5.0mL |
1.0mL |
14.0mL |
10.0mL |
5 |
30.0mL |
5.0mL |
1.0mL |
4.0mL |
10.0mL |
➁ 50mL 비커에 조재한 용액을 앞서 제시한 표를 활용하여 각각 정량을 취한다.
➂ 초시계를 준비한 뒤 반응 플라스크에 마그네틱 바를 넣고 교반기를 작동시킨다.
➃ 실험 시 반응 시작 시간을 기록하고 50mL 비커 속의 용액을 신속하게 반응 플라스크에 가한다.
➄ 반응 용액이 변화가 이뤄젔을 때 시간을 기록한다.
- 실험 결과
▶ 시계 반응 시 사용되는 반응
1단계와 2단계 반응식은 다음과 같다.
(보기 쉽게 정리하였습니다.)
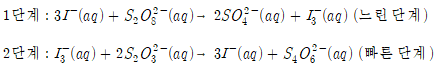
▶ 반응 속도
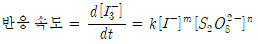
- 실험실 온도는 18℃로 일정하였다.
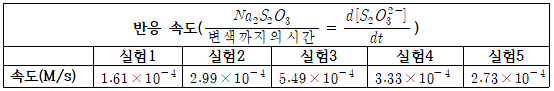
- 반응속도는 변색까지의 시간에 대한 Na2S2O3의 값으로 다음과 같다. (보기 쉽게 정리하였습니다.)

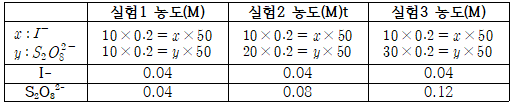
| 반응 | 반응 플라스크 속의 초기 농도 | |||
| I | S2O8(2-) | |||
| 1 | 0.04 | 0.04 | 311 | 0.322 |
| 2 | 0.04 | 0.08 | 167 | 0.599 |
| 3 | 0.04 | 0.12 | 91 | 1.1 |
| 4 | 0.08 | 0.04 | 150 | 0.667 |
| 5 | 0.12 | 0.04 | 183 | 0.546 |
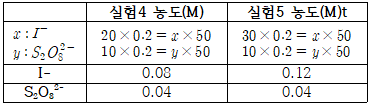
▶ 반응 실험 1, 2, 4 m값, n값 구하기 (보기 쉽게 정리하였습니다.)
- m값 구하기 (1,4)

- n값 구하기 (1,2)

- 결과
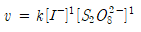
▶ k값 구하기
- 실험 1
8.05×0.00001 = k[0.04]^(1)[0.04]^(1)
k = 0.0503125.... (보기 쉽게 정리하겠습니다.)

반응형
'3학년' 카테고리의 다른 글
| 액체의 밀도 측정 예비레포트 (0) | 2020.03.28 |
|---|---|
| 활성탄에 의한 아세트산 흡착 결과레포트 (0) | 2020.03.26 |
| 시계반응 예비레포트 (0) | 2020.03.23 |
| 반응속도상수 결과레포트 (0) | 2020.03.22 |
| 속도상수 예비레포트 (0) | 2020.03.21 |



